
Das follikuläre Lymphom (FL) ist eine bösartige Erkrankung des lymphatischen Systems und eine Unterform der Non-Hodgkin-Lymphome.1 Es entsteht aus B-Lymphozyten, die sich unkontrolliert vor allem in den Lymphknoten, aber auch im Knochenmark vermehren. Seltener findet man diese bösartigen Zellen im Blut, in der Milz oder in den Schleimhäuten.2
Das follikuläre Lymphom gehört zu den langsam wachsenden (= indolenten) Lymphomen. In seltenen Fällen kann sich das Wachstum der Zellen jedoch verändern, sodass sich die Lymphomzellen immer schneller teilen.2

Follikuläre Lymphome machen rund 25 % aller Non-Hodgkin-Lymphome aus. In Europa stellen sie die zweithäufigste Form der malignen (bösartigen) Lymphome dar. Im Vergleich zu anderen Krebserkrankungen wie etwa Brust- oder Darmkrebs ist das follikuläre Lymphom aber eine eher seltene Erkrankung.1 In den Jahren 2013/2014 wurden in Deutschland jährlich etwa 3100 follikuläre Lymphome diagnostiziert, wobei Frauen etwas häufiger (53 %) betroffen waren als Männer (47 %). Bei der Diagnosestellung waren die Patienten durchschnittlich 66 Jahre alt.3
In den Ländern der westlichen Welt erkranken etwa drei bis fünf Menschen pro 100.000 Einwohner pro Jahr an einem follikulären Lymphom, wobei die Häufigkeit in den letzten Jahren zugenommen hat.4
Die genauen Ursachen der Erkrankung sind bisher nicht geklärt. Die Tumorzellen des follikulären Lymphoms zeigen Veränderungen in ihren Genen, man weiß jedoch nicht genau, wodurch diese entstehen.1
Eine typische Erbgutveränderung bei follikulären Lymphomen ist die sogenannte Translokation t(14;18) in einem B-Lymphozyten. Hierbei bricht sowohl bei einem Chromosom (siehe Infokasten) mit der Nummer 14 als auch bei Chromosom 18 ein Teil ab und fügt sich beim jeweils anderen Chromosom wieder an.
Durch diese Translokation geraten die natürlichen Funktionen des betroffenen B-Lymphozyten außer Kontrolle, sodass die Zelle nicht nach der üblichen Zeit zugrunde geht, sondern sich teilt und den Fehler an alle Tochterzellen weitergibt. Im Gegensatz zu gesunden B-Zellen sind die durch die Translokation veränderten Tumorzellen als Abwehrzellen nicht mehr tauglich.1
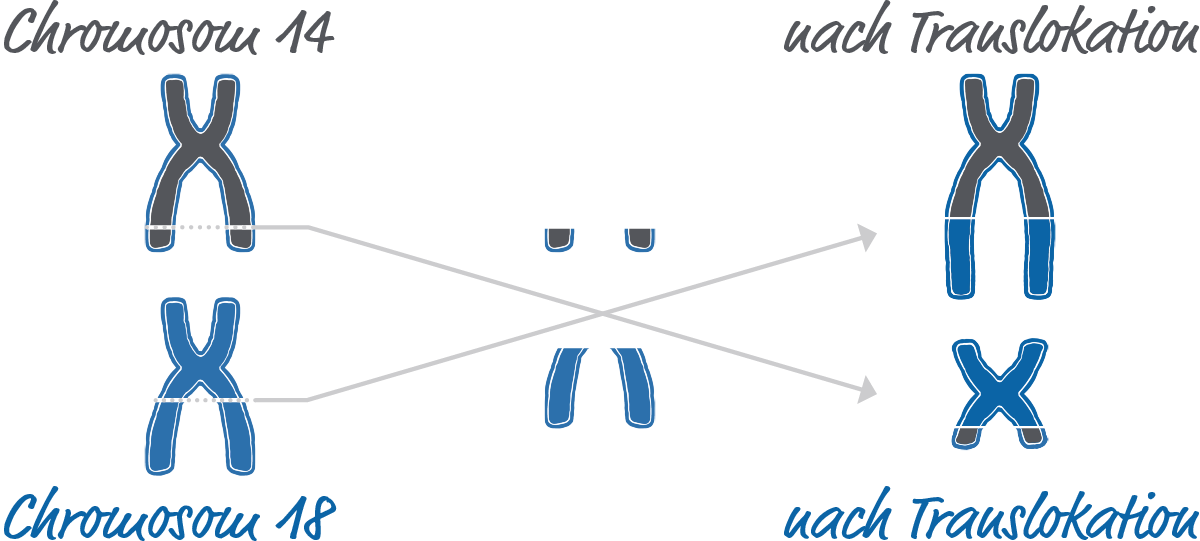

Chromosomen sind Strukturen in menschlichen Zellen, die die Erbinformation speichern. Sie bestehen aus DNA und enthalten Gene, über die bestimmte Eigenschaften vererbt werden. Gesunde menschliche Zellen enthalten normalerweise insgesamt 46 Chromosomen. Dabei kommt jedes Chromosom doppelt vor. Die menschlichen Chromosomen werden von 1 bis 22 (plus zwei Geschlechtschromosomen) durchnummeriert.
Verschiedene Studien weisen darauf hin, dass bestimmte Faktoren das Risiko, an einem follikulären Lymphom zu erkranken, erhöhen. Dazu zählen:5

Wenn das maligne Lymphom das Knochenmark befällt, kann es zu Störungen der Blutbildung kommen, beispielsweise zur Blutarmut (Anämie) oder zu einem Mangel an weißen Blutzellen (Leukozyten). Betroffene Patienten klagen über Müdigkeit, Leistungsschwäche oder Infektanfälligkeit. Ein Mangel an Blutplättchen (Thrombozyten) kann dazu führen, dass Patienten Blutergüsse („blaue Flecken“) ohne erkennbare Ursache bekommen, bei kleinen Verletzungen lange bluten oder kleine Blutpünktchen insbesondere an den Füßen und Beinen aufweisen.1,2

Besteht der Verdacht, dass ein follikuläres Lymphom (FL) vorliegen könnte (etwa weil ein Patient Lymphknotenschwellungen hat, die seit Wochen bestehen oder zunehmen), sollte ein Lymphknoten entnommen und von einem entsprechend erfahrenen Pathologen feingeweblich (histologisch) untersucht werden.4 Hierfür sollte möglichst ein kompletter Lymphknoten operativ entnommen werden. Ist das nicht möglich, weil ein betroffener Lymphknoten nur schwer zugänglich ist, können alternativ auch größere Gewebeproben mithilfe einer Stanzbiopsie gewonnen werden.1
Der Pathologe stuft den Reifegrad der FL-Zellen anhand ihrer Zentroblastenanteile in verschiedene Reifegrade ein (Zentroblasten sind eine Stufe bei der Zellteilung von Lymphozyten). Dies wird als „Grading“ bezeichnet. Es gibt die Grade 1, 2, 3A oder 3B. Ein follikuläres Lymphom mit dem Grad 1, 2 oder 3A gilt als indolent (= langsam wachsend), ein FL mit dem Grad 3B wird als aggressives (= schnell wachsendes) Lymphom eingestuft.1,5

Anamnese (Erhebung der Krankengeschichte)

Körperliche Untersuchung, wobei der Arzt insbesondere auf Lymphknoten sowie die Größe von Leber und Milz achtet
Bildgebende Verfahren (z. B. Computertomografie von Hals, Brustraum und Bauch; evtl. Ultraschall oder Röntgen)

Laboruntersuchungen
Ob und wie ein Patient mit follikulärem Lymphom behandelt werden muss, richtet sich nach dem Ausbreitungsstadium gemäß der Ann-Arbor-Klassifikation. Ärzte unterscheiden dabei vier Stadien:5
Liegt eine Beteiligung von Organen und Geweben außerhalb der Lymphknoten vor, wird das mit einem „E“ gekennzeichnet (E steht für extranodal, was „außerhalb von Lymphknoten“ bedeutet).
Zusätzlich zum Stadium wird angegeben, ob der Patient sogenannte B-Symptome aufweist (Fieber, Gewichtsverlust oder Nachtschweiß). Der Zusatz „A“ bedeutet, dass der Patient keine B-Symptome hat; „B“ sagt aus, dass bei dem Patienten B-Symptome vorliegen.2
Mithilfe des „Follicular Lymphoma International Prognostic Index“ (FLIPI) kann der Arzt den wahrscheinlichen Krankheitsverlauf – also die „Prognose“ des Patienten – abschätzen. Dazu benötigt der Arzt Informationen zu folgenden Risikofaktoren:3,5
Jedem dieser Risikofaktoren wird ein Punkt gegeben. Je mehr dieser Risikofaktoren vorliegen, desto ungünstiger dürfte die Erkrankung verlaufen. Das Risikoprofil eines Patienten hat jedoch derzeit außerhalb von klinischen Studien keinen großen Einfluss auf die Festlegung seiner Behandlung.1
Patienten mit follikulärem Lymphom sollten sich durch Fachärzte für Hämatologie und Onkologie (in Kliniken tätige oder niedergelassene Ärzte) behandeln lassen. Empfehlenswert ist die Therapie innerhalb von klinischen Studien, die deutschlandweit an vielen Behandlungszentren angeboten werden.2 Bei Teilnahme an einer klinischen Studie kann der Patient davon ausgehen, dass er nach neuestem Wissensstand behandelt wird.
Für die Therapie follikulärer Lymphome stehen verschiedene Behandlungsmöglichkeiten zur Verfügung, beispielsweise Strahlentherapie, Immunchemotherapie, zielgerichtete Therapien, eine Stammzelltransplantation oder eine CAR-T-Zelltherapie.1
Die Wahl der geeigneten Therapie richtet sich u. a. nach dem Krankheitsstadium entsprechend der Ann-Arbor-Klassifikation, dem Allgemeinzustand und eventuell vorliegenden Begleiterkrankungen des Patienten.5 Bei manchen Patienten muss nicht sofort mit der Behandlung begonnen werden, sondern es genügt, wenn der Arzt sie zunächst beobachtet. Mediziner bezeichnen dies als „Watch & Wait“-Strategie.4
Die Behandlung des follikulären Lymphoms hängt davon ab, wie weit sich die Erkrankung bei der Diagnosestellung bereits ausgebreitet hat.
In den Stadien I und II nach der Ann-Arbor-Klassifikation ist die Bestrahlung der betroffenen Lymphknotenregion eine effektive Behandlungsmethode.4 Da es bei einer alleinigen Strahlentherapie jedoch zu Krankheitsrückfällen außerhalb des Bestrahlungsgebiets kommen kann, empfehlen Ärzte je nach Situation eine Kombination aus Strahlentherapie plus Chemo- oder Antikörpertherapie, um dem Patienten eine Chance auf Heilung zu ermöglichen.3,4
Wird die Erkrankung erst sehr spät diagnostiziert (Stadien III und IV nach der Ann-Arbor-Klassifikation), verfolgt die Therapie das Ziel, krankheitsbedingte Symptome zu lindern und die Krankheit möglichst zurückzudrängen.4 Für die Wahl der geeigneten Therapie ist die sogenannte Tumorlast des Patienten von Bedeutung:
Keine Beschwerden, geringe Tumorlast: Da viele follikuläre Lymphome indolent verlaufen – also nur langsam voranschreiten –, ist auch im Stadium III und IV ein abwartendes Beobachten möglich (auch „Watch & Wait“ genannt), solange der Patient keine Beschwerden hat und seine Tumorlast gering ist.4 Eine Untersuchung ergab, dass die Watch & Wait-Strategie für Patienten ohne Symptome keinen Nachteil bedeutet.4
Beschwerden und/oder hohe Tumorlast: Bei Patienten im Stadium III oder IV, die Symptome wie Blutarmut, Fieber oder Gewichtsverlust und/oder eine hohe Tumorlast haben, soll eine Therapie eingeleitet werden. Experten empfehlen eine kombinierte Behandlung mit einem sogenannten Anti-CD20-Antikörper plus Chemotherapie.3,4 Diese Kombinationsbehandlung wird als Immunchemotherapie bezeichnet. Diese Kombinationsbehandlung kann zu einer Besserung der Krankheitszeichen führen. Anschließend soll eine sogenannte Erhaltungstherapie mit einem Anti-CD20-Antikörper über zwei Jahre erfolgen.2,4
Die Tumorlast ist ein Maß für die Menge an Krebszellen im Körper. Eine hohe Tumorlast liegt bei einem Patienten mit follikulärem Lymphom beispielsweise dann vor, wenn er sehr stark vergrößerte Lymphknoten mit einem Durchmesser von über 7 cm hat.3
Manche Tumorzellen tragen auf ihrer Oberfläche bestimmte Merkmale wie z. B. das CD20-Oberflächenantigen, das auf gesunden Zellen nicht oder deutlich weniger vorkommt. Das CD20-Antigen ist auf Tumorzellen von follikulären Lymphomen oft in großer Zahl vorhanden.6
Derzeit ist davon auszugehen, dass follikuläre Lymphome im Stadium III und IV nicht geheilt werden können und dass mit Krankheitsrückfällen (Rezidiven) zu rechnen ist. Wenn ein Rezidiv auftritt, soll erneut eine Lymphknotenuntersuchung erfolgen, da indolente follikuläre Lymphome manchmal in aggressive follikuläre Lymphome übergehen können.2,4 Darüber hinaus wird der Arzt bei einem Krankheitsrückfall weitere diagnostische Tests veranlassen, um das Ausmaß des Rezidivs bestimmen zu können.2,3
Die Wahl der Rezidivtherapie hängt von verschiedenen Faktoren ab, u. a. von der Art der Vortherapie und der Erhaltungstherapie sowie vom Zeitpunkt des Rezidivs.
Tritt der Krankheitsrückfall mehr als zwei Jahre nach einer Immunchemotherapie auf, kann oft erneut mit einer Immunchemotherapie behandelt werden.3 Falls diese nicht mehr so gut wirkt wie in der Erstlinientherapie, kann ein Wechsel des Antikörpers sinnvoll sein.4
Bei einem Rezidiv, das weniger als zwei Jahre nach Beginn einer Immunchemotherapie auftritt, können bei jüngeren, fitten Patienten andere Behandlungsverfahren eingesetzt werden, beispielsweise eine Hochdosis-Chemotherapie mit anschließender autologer Stammzelltransplantation.2,4 Bei der autologen Stammzelltransplantation kommen die Spenderzellen vom Patienten selbst.
Für jüngere, fitte FL-Patienten, die nach einer autologen Stammzelltransplantation ein Rezidiv entwickelt haben und/oder die auf eine Chemotherapie nicht ansprechen, kann eine allogene Stammzelltransplantation in Betracht gezogen werden.3 Bei der allogenen Stammzelltransplantation stammen die Stammzellen von einer anderen Person.
Die CAR-T-Zelltherapie ist eine innovative Therapieoption, bei der gentechnisch veränderte Immunzellen des Patienten zum Einsatz kommen.7,8 Dadurch erhalten die T-Zellen den sogenannten chimären Antigenrezeptor (CAR) auf ihrer Oberfläche und können damit Krebszellen als Bedrohung für den Körper identifizieren und töten.
In den vergangenen Jahren entwickelten Forscher verschiedene neue Medikamente für die Therapie bösartiger Lymphome. Einige dieser neuen Wirkstoffe zeigten in Studien vielversprechende Ergebnisse; manche davon können unter bestimmten Voraussetzungen auch bei Patienten mit follikulärem Lymphom im Rezidiv eingesetzt werden.4 Ob eine solche neue Substanz im Einzelfall infrage kommt, wird der Hämatologe/Onkologe mit dem betroffenen Patienten besprechen.
Nach der Therapie beginnt für alle Patienten ein engmaschiges Nachsorgeprogramm. Bei beschwerdefreien (asymptomatischen) Patienten sollten in den ersten beiden Jahren alle drei Monate Kontrolluntersuchungen durchgeführt werden, ab dem dritten Jahr dann alle sechs Monate.3
Da follikuläre Lymphome durch die aktuell verfügbaren Therapien meist nur für eine bestimmte Zeit zurückgedrängt werden können, sollte regelmäßig kontrolliert werden, ob ein Krankheitsrückfall eingetreten ist. Falls ja, kann rasch eine geeignete Behandlung eingeleitet werden. Bei den Nachsorgeuntersuchungen achtet der Arzt auch darauf, ob die Therapie zu Langzeitfolgen (z. B. Herzproblemen, Zweittumor) geführt hat.1
Die Nachsorgeuntersuchungen setzen sich aus verschiedenen Komponenten zusammen:3

Anamnese und körperliche Untersuchung: Der Arzt befragt den Patienten ausführlich zu seinem Befinden (neu aufgetretene Lymphknotenschwellungen oder Beschwerden, z. B. B-Symptome wie Fieber, Gewichtsverlust oder Nachtschweiß) und führt eine gründliche körperliche Untersuchung durch. Dabei tastet er die verschiedenen Lymphknotenstationen beispielsweise am Hals, in den Achseln und in der Leistengegend sowie den Bauch ab.3

Blutentnahme: Der Arzt untersucht die Zusammensetzung des Blutes und kann die Anzahl der verschiedenen im Blut vorhandenen Zellen sowie weitere Blutwerte bestimmen.3
Je nach Situation können weitere Untersuchungen durchgeführt werden wie etwa eine Computertomografie (CT) oder Ultraschall- bzw. Röntgenuntersuchungen.3
Bitte beachten Sie, dass die auf dieser Website aufgelisteten Therapieoptionen ausschließlich Ihren Informationszwecken dienen und keinen Anspruch auf fachliche Vollständigkeit bieten.
Diese Informationen stellen daher keinen Ersatz für eine individuelle Beratungs- oder Behandlungsleistung, Empfehlung oder medizinische Diagnose durch einen Arzt dar und dienen keinesfalls der Selbstdiagnose.
Abkürzungen
CAR: Chimeric Antigen Receptor
CT: Chemotherapie
FL: follikuläres Lymphom
WHO: Weltgesundheitsorganisation
Quellen